ЛИТОСФЕРА
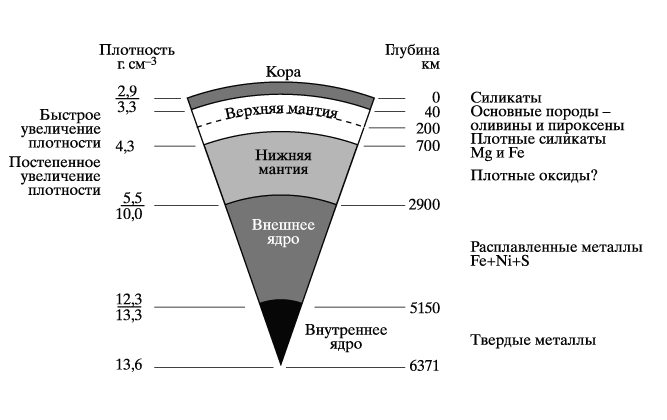
ЛИТОСФЕРА – внешняя сфера «твердой» Земли, включающая земную кору и часть верхней мантии (рис. 1).
Толщина коры под континентами составляет, в среднем, 35–40 км. Там, где на суше расположены молодые высокие горы, она часто превышает 50 км (например, под Гималаями достигает 90 км). Под океанами кора более тонкая – в среднем около 7–10 км, а в некоторых районах Тихого океана – всего 5 км.
Границы земной коры определяются по скорости распространения сейсмических волн. Сейсмические волны дают информацию и о свойствах мантии. Установлено, что верхняя мантия состоит, главным образом, из силикатов магния и железа. Состав нижней мантии остается загадкой, однако высказывается предположение, что она содержит оксиды магния и кремния. Заключения о составе земного ядра были сделаны на основании не только анализа сейсмических волн, но и расчетов плотности и изучения состава метеоритов. Считается, что внутреннее ядро представляет собой твердый сплав железа и никеля. Внешнее ядро, по-видимому, жидкое и имеет несколько меньшую плотность. Некоторые специалисты считают, что оно содержит до 14% серы.
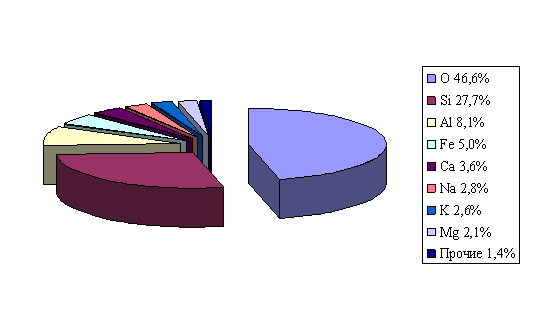
Земная кора, гидросфера и атмосфера образовались, в основном, в результате высвобождения веществ из верхней мантии молодой Земли. Сейчас время в срединных хребтах на дне океанов продолжается формирование океанической коры, сопровождающееся выделением газов и небольших количеств воды. По-видимому, и образование коры на молодой Земле было результатом подобных процессов, вследствие чего сформировалась тонкая оболочка, составляющая менее 0,0001% объема всей планеты. Состав этой оболочки, образующей континентальную и океаническую кору, изменялся во времени, прежде всего, за счет перехода элементов из мантии из-за частичного плавления на глубине примерно 100 км. Средний химический состав современной земной коры характеризуется большим содержанием кислорода, за которым следуют кремний и алюминий (рис. 2).
Средние значения относительного содержания химических элементов в верхнем слое земной коры по предложению советского геохимика А.Е.Ферсмана (1883–1945) называют кларками элементов в честь американского ученого Франка Уилгсуорта Кларка (1847–1931), который разработал методы количественной оценки распространенности химических элементов.
Анализ значений кларков позволяет понять многие закономерности распределения химических элементов. Кларки химических элементов земной коры различаются более чем на десять порядков. Так, если алюминия в земной коре содержится более восьми процентов по массе, то, например, золота 4,3·10-7 %, меди – 5·10-3 %, урана – 3·10–4%, а такого редкого металла, как рений – всего 7·10–8 %.Элементы, содержащиеся в относительно большом количестве, образуют в природе многочисленные самостоятельные химические соединения, а элементы с малыми кларками рассеяны, преимущественно, среди химических соединений других элементов. Элементы, кларки которых меньше 0,01%, называют редкими.
Основными соединениями, образующими литосферу, являются диоксид кремния, силикаты и алюмосиликаты. Бóльшую часть литосферы составляют кристаллические вещества, образовавшиеся при охлаждении магмы – расплавленного вещества в глубинах Земли. При остывании магмы образовывались и горячие растворы. Проходя по трещинам в окружающих горных породах, они охлаждались и выделяли содержащиеся в них вещества.
Поскольку некоторые минералы стабильны только при определенных условиях, при изменении температуры и давления они распадаются. Например, ряд силикатов, образующихся глубоко в коре при высоких температуре и давлении, становятся неустойчивыми, когда попадают на поверхность Земли. С другой стороны, на большой глубине под действием внутреннего тепла Земли и повышенного давления многие горные породы меняют свой вид, образуя новые кристаллические формы.
Поверхность континентальной коры подвержена действию атмосферы и гидросферы, что выражается в процессах выветривания. Физическое выветривание является механическим процессом, в результате которого порода размельчается до частиц меньшего размера без существенных изменений в химическом составе. Химическое выветривание приводит к образованию новых веществ, оно происходит под действием влаги, особенно подкисленной, и некоторых газов (например, кислорода), разрушающих минералы.
Простейший процесс выветривания – это растворение минералов. Вода вызывает разрыв ионных связей, соединяющих, например, катионы натрия и хлорид ионы в галите NaCl. В этом процессе не участвуют катионы водорода, поэтому он не зависит от рН.
При разрушении веществ, содержащих элементы в низких степенях окисления, например, сульфидов, большую роль играет кислород. В эти процессы часто вовлечены микроорганизмы. Так, окисление пирита FeS2 можно моделировать следующим рядом реакций. Сначала окисляется сера(–I):
2FeS2 + 2H2O + 7O2 = 4H+ + 4SO42– + 2Fe2+
Затем следует окисление железа(II), катализируемое железоокисляющими бактериями:
4Fe2+ + O2 + 6H2O = 4FeO(OH) + 8H+
Образующийся гетит FeO(OH) покрывает дно ручьев в виде характерного желто-оранжевого налета.
Железоокисляющие бактерии извлекают энергию при окислении неорганических веществ, поэтому они развиваются там, где нет органических соединений, используя в качестве источника углерода СО2. Однако окисление железа – не очень эффективный способ выработки энергии: для получения 1 г клеточного углерода должно быть окислено примерно 220 г железа(II). В результате там, где живут железоокисляющие бактерии, образуются большие отложения соединений железа(III).
Выветривание карбонатных минералов, например CaCO3, происходит при взаимодействии с кислотами, содержащимися в воде за счет поглощения диоксида углерода, а также антропогенного диоксида серы. При этом поверхностные воды нейтрализуются и обогащаются гидрокарбонат-ионами:
CaCO3 + H2CO3 = Ca2+ + 2HCO3–
Разрушение силикатов, например Mg2SiO4 (форстерит) можно описать следующим уравнением:
Mg2SiO4 + 4H2CO3 = 2Mg2+ + 4HCO3– + H4SiO4
Реакция идет за счет образования чрезвычайно слабой ортокремниевой кислоты, при этом минерал со временем полностью растворяется. Однако при выветривании более сложных силикатов растворимыми оказываются не все продукты. В общем случае в результате выветривания образуются, в основном, кварц и глинистые минералы – водосодержащие слоистые алюмосиликаты. Например, при выветривании CaAl2Si2O8 (анортит) твердым продуктом реакции является глинистый минерал каолинит:
CaAl2Si2O8 + 2H2CO3 + H2O = Ca2+ + 2HCO3– + Al2Si2O5(OH)4
На скорость выветривания влияет биосфера (где создается диоксид углерода), а также рельеф суши и климат, состав воды, тип материнской породы и кинетика реакций с участием отдельных минералов. Так, во влажных тропиках выветривание происходит быстрее. Это связано с тем, что высокие температуры ускоряют реакции, а постоянные ливни делают возможным быстрое вымывание и снос в моря и океаны даже практически нерастворимых соединений, например, оксидов алюминия и железа.
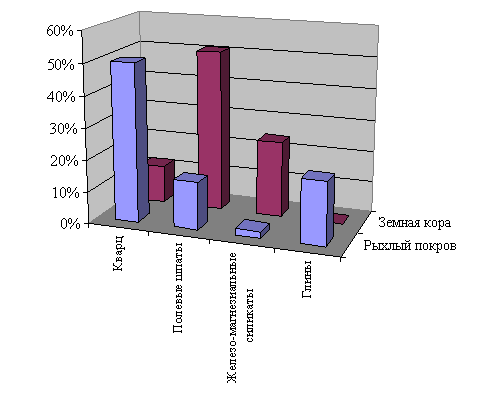
Продукты выветривания образуют рыхлые континентальные отложения, мощность которых меняется от 10–20 см на крутых склонах до десятков метров на равнинах и сотен метров – во впадинах. Средний минералогический состав рыхлого покрова суши заметно отличается от состава земной коры континентов (рис. 3).
На рыхлых покровных отложениях сформировались почвы, играющие важнейшую роль во взаимодействии живых организмов с земной корой. В почвах систематически консервируется значительная масса органического вещества, синтезированного высшими растениями. Окисление органического вещества в почвах катализируется ферментами микроорганизмов, при этом образуется диоксид углерода, который при взаимодействии с водой дает слабую угольную кислоту. Это может понизить рН почв до 4–5, что оказывает существенное влияние на процессы выветривания. Почва участвует в круговороте азота, серы и фосфора, а также многих металлов. Поэтому проблема охраны почв имеет большое значение.
На ранних этапах истории человечества деятельность людей почти не затрагивала глубины Земли. Однако с началом бурного развития промышленности резко возросли потребности человека в полезных ископаемых. Их добыча и переработка начали оказывать вредное воздействие на природу. При разработке открытых горных выработок образуется много пыли, загрязняющей окрестности. Огромные площади занимают отвалы «пустой» породы, образующиеся при добыче твердых полезных ископаемых. Откачка воды из горных выработок приводит к образованию подземных пустот. Многие горнодобывающие предприятия сбрасывают в реки недостаточно очищенные стоки, что ведет к загрязнению природных вод. В окружающую среду попадают вредные вещества из отвалов этих предприятий. Немало опасных веществ рассеивается при транспортировке руд и продуктов их переработки.
Загрязнение окружающей среды в результате добычи и переработки полезных ископаемых можно уменьшить, если использовать достижения науки и более совершенные технологии.
Елена Савинкина
Ревель П., Ревель Ч. Среда нашего обитания. В четырех книгах (перевод с англ.). М., Мир, 1995
Химия и общество (перевод с англ.) М., Мир, 1995
Добровольский В.В. Основы биогеохимии. Учеб. пособие для геогр., биол., геол., с.-х. спец. вузов. М., Высш. шк., 1998
Андруз Дж., Бримблекумб П., Джикелз Т., Лисс П. Введение в химию окружающей среды (перевод с англ.). М., Мир, 1999
Ответь на вопросы викторины «Неизвестные подробности»